专注细胞治疗,打造全流程解决方案
加速细胞治疗从实验室规模到商业化进程
随着2017年诺华的CAR-T产品Kymriah作为全球第一支被FDA批准上市的细胞治疗药物,细胞治疗的风潮便席卷全球。在2020年,中国医药市场上也上市了两款针对靶点CD19的CAR-T药物。与传统蛋白类(抗体类,重组蛋白类)药物研发,生产的工艺与周期不同,细胞治疗药物因其理化性质敏感,平台工艺积累还不成熟,检测与工艺设备耗材供应商分开提供各自产品与解决方案等原因面临工艺开发优化平台不稳定,周期较长,细胞终端产品无法灭菌/除菌过滤,需要完整的封闭系统且容易实现线性放大,工艺开发放大与QC检测需要接触多家供应商,从设备考察,选型,到投入使用周期较长,且对接容易出现偏差等问题。
赛多利斯基于实验室产品与生物工艺产品,从早期分子靶点开发研究到平台工艺优化放大,从上游细胞病毒培养下游过滤层析纯化到过程监控与QC检测,从产品服务到技术验证服务。
了解我们的解决方案
了解我们的细胞治疗工艺方案
广义细胞治疗(Cell Therapy)包含有基因编辑的细胞治疗(Gene Modified Cell Therapy)与非基因编辑的细胞治疗(Non Gene Modified Cell Therapy)。针对GMCT ,可提供慢病毒载体(LV),修饰后的体细胞从给实验室规模到GMP生产规模,从上游病毒包装到下游纯化多维度的工艺推荐方案与相应产品,对于NGMCT,同样也可提供从工艺开发,到大规模商业化制备,从上游到下游的工艺开发服务与产品,此外还提供针对QC检测,验证等专业性深度服务。
根据细胞类型分类
MSC的全工艺流程可以从实验室阶段开始的早期分子靶点功能和表型表征研究,进入到小试阶段的工艺开发与优化,最后进入产业化生产阶段。对于每一个阶段的任务,赛多利斯都有对应的解决方案,加速MSC产品的上市进程。
MSC 全工艺流程:
细胞获取与分离-MSC扩增-MSC收获与纯化-MSC制剂与灌装-MSC保存
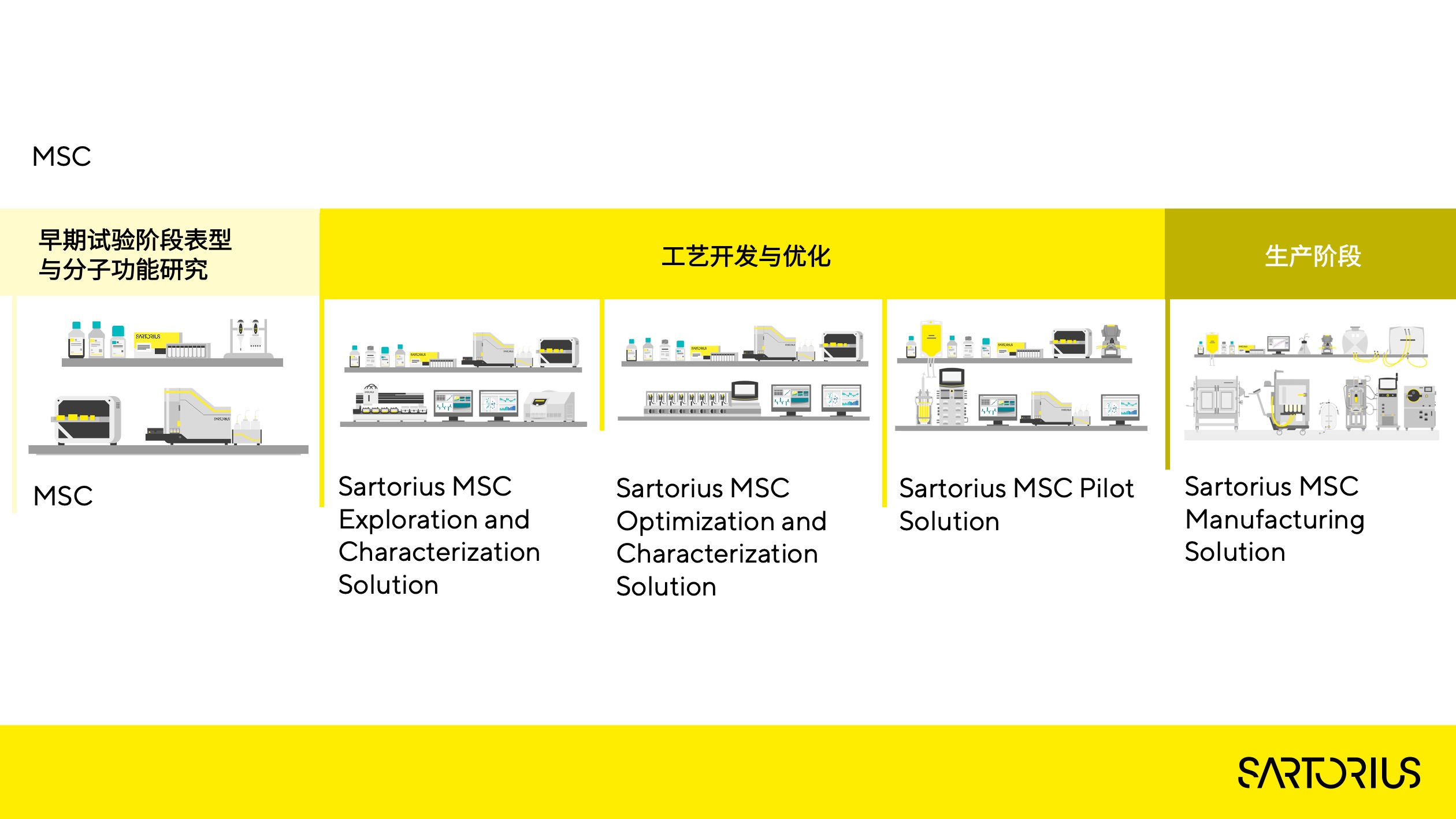
客户的需求
MSC 在早期实验室阶段进行表型与分子功能研究时需要高效,准确,定量且快速的自动化分析在小试阶段进行工艺开发时,需要依据CQA(关键质量属性)进行CPP(关键工艺参数)的探索与优化,确定稳健的工艺参数范围。
由于MSC无法进行终端灭菌与除菌过滤,根据合规要求终端产品必须无菌,因此在产业化规模下制备MSC药品是要求封闭系统的。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于MSC药物的上市进程无疑是一种阻力。
我们的解决方案
赛多利斯Ique 3与Incucyte® SX5针对MSC 在早期实验室阶段进行表型与分子功能研究可提供需要高效,准确,定量且快速的自动化分析,在小试阶段进行工艺开发时,Ambr®15&250可对于细胞培养的条件进行的探索与优化,针对MSC的培养基MSC NutriStem® XF可提高细胞密度,确定稳健的工艺参数范围。
由于MSC无法进行终端灭菌与除菌过滤,根据合规要求终端产品必须无菌,因此在产业化规模下制备MSC药品是要求封闭系统的,我们的一次性产品涵盖上游下游,小规模至大规模阶段,在MSC制备的不同阶段都可提供封闭的,一次性应用的方案。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于MSC药物的上市进程无疑是一种阻力,因此一站式设备与技术的服务方案,可省去不必要的沟通时间;在每个阶段我们就为您考虑到下一个阶段快速推进方案,加速您的药品上市进程。
iPSC的全工艺流程可以从实验室阶段开始的早期分子靶点功能和表型表征研究,进入到小试阶段的工艺开发与优化,最后进入产业化生产阶段。对于每一个阶段的任务,赛多利斯都有对应的解决方案,加速iPSC产品的上市进程。
iPSC 全工艺流程:
细胞获取与分离 - 扩增 - 收获与纯化 - 制剂与灌装 - 保存
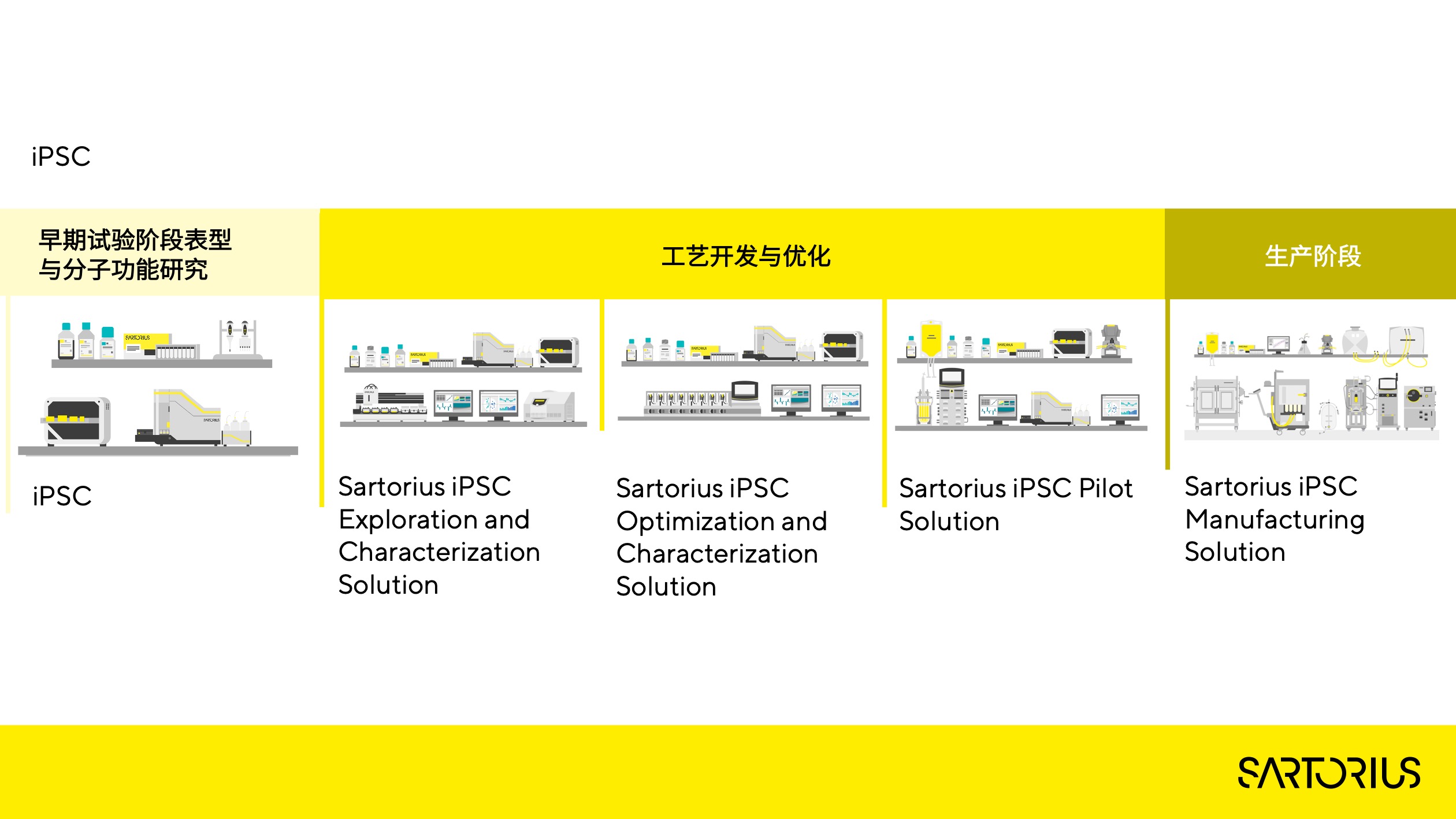
客户的需求
iPSC 在早期实验室阶段进行表型与分子功能研究时需要高效,准确,定量且快速的自动化分析
在小试阶段进行工艺开发时,需要依据CQA(关键质量属性)进行CPP(关键工艺参数)的探索与优化,确定稳健的工艺参数范围。
由于iPSC无法进行终端灭菌与除菌过滤,根据合规要求终端产品必须无菌,因此在产业化规模下制备iPSC药品是要求封闭系统的,从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于iPSC药物的上市进程无疑是一种阻力。
我们的解决方案
赛多利斯的Ique3与Incucyte® SX5针对iPSC 在早期实验室阶段进行表型与分子功能研究可提供需要高效,准确,定量且快速的自动化分析,在小试阶段进行工艺开发时,Ambr® 15,250可对于细胞培养的条件进行的探索与优化,针对iPSC的培养基NutriStem® hPSC XF可提高细胞密度,确定稳健的工艺参数范围。
由于iPSC无法进行终端灭菌与除菌过滤,根据合规要求终端产品必须无菌,因此在产业化规模下制备iPSC药品是要求封闭系统的,我们的一次性产品涵盖上游下游,小规模至大规模阶段,在iPSC制备的不同阶段都可提供封闭的,一次性应用的方案。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于iPSC药物的上市进程无疑是一种阻力,因此一站式设备与技术的服务方案,可省去不必要的沟通时间;在每个阶段我们就为您考虑到下一个阶段快速推进方案,加速您的药品上市进程。
T细胞的全工艺流程可以从实验室阶段开始的早期分子靶点功能和表型表征研究,进入到小试阶段的工艺开发与优化,最后进入产业化生产阶段。对于每一个阶段的任务,赛多利斯都有对应的解决方案,加速T细胞产品的上市进程。
CAR-T 全工艺流程:
外周血采样 - T细胞筛选与清洁 - 转导 - 扩增 - 收获与灌装 - 检测 - 给药
客户的需求
CAR-T 在早期实验室阶段进行表型与分子功能研究时需要快速,高效,准确定量的自动化分析
在小试阶段进行工艺开发时,需要依据CQA(关键质量属性)进行CPP(关键工艺参数)的探索与优化,确定稳健的工艺参数范围。
由于CAR-T产品无法进行终端灭菌与除菌过滤,根据合规要求终端产品必须无菌,因此在产业化规模下制备CAR-T药品是要求封闭系统的。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于CAR-T药物的上市进程无疑是一种阻力。
我们的解决方案
赛多利斯的Ique® 3与Incucyte® SX5针对CAR-T 在早期实验室阶段进行表型与分子功能研究可提供需要高效,准确,定量且快速的自动化分析,在小试阶段进行工艺开发时,Ambr® 15&250可对于细胞培养的条件进行的探索与优化,针对CAR-T的培养基4cell® Nutri-T可提高细胞密度,确定稳健的工艺参数范围。
由于CAR-T无法进行终端灭菌与除菌过滤,根据合规要求终端产品必须无菌,因此在产业化规模下制备CAR-T药品是要求封闭系统的,我们的一次性产品涵盖上游下游,小规模至大规模阶段,在CAR-T制备的不同阶段都可提供封闭的,一次性应用的方案。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于CAR-T药物的上市进程无疑是一种阻力,因此一站式设备与技术的服务方案,可省去不必要的沟通时间;在每个阶段我们就为您考虑到下一个阶段快速推进方案,加速您的药品上市进程。
慢病毒载体(LV)的全工艺流程可以从实验室阶段开始的早期分子靶点功能和表型表征研究,进入到小试阶段的工艺开发与优化,最后进入产业化生产阶段。对于每一个阶段的任务,赛多利斯都有对应的解决方案,加速慢病毒载体产业化规模进程。
LV 全工艺流程:
细胞扩增-病毒制备-病毒收获澄清-超滤浓缩换液-捕获层析-超滤浓缩换液-除菌过滤-终端灌装保存
客户的需求
慢病毒在早期实验室阶段进行表型与分子功能研究时需要快速,高效,准确定量的自动化分析
在小试阶段进行工艺开发时,需要依据CQA(关键质量属性)进行CPP(关键工艺参数)的探索与优化,确定稳健的工艺参数范围。
由于贴壁模式制备慢病毒在放大性与产量方面有所限制,慢病毒的上游培养由贴壁模式转换到悬浮模式需求日益强烈。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于CAR-T药物的上市进程无疑是一种阻力。
我们的解决方案
我们的Ique3与Incucyte® SX5针对LV 在早期实验室阶段进行表型与分子功能研究可提供需要高效,准确,定量且快速的自动化分析,
在小试阶段进行工艺开发时,Ambr® 15&250可对于细胞培养的条件进行的探索与优化,针对HEK293的培养基XCELL HEK293可提高细胞密度,确定稳健的工艺参数范围。
LV 上游工艺由Ambr®系列进行悬浮培养工艺开发优化,可悬浮培养线性放大至RM或STR一次性生物反应器中,同时在产业化规模下制备慢病毒载体实现封闭系统下,灭除清洗验证;我们的一次性产品涵盖上游下游,小规模至大规模阶段,在慢病毒载体制备的不同阶段都可提供封闭的,一次性应用的方案。
从早期试验时研发到大规模生产,每个阶段不同的设备,方案供应商的衔接与沟通需要花费大量的时间成本,对于慢病毒的产业化进程无疑是一种阻力,因此一站式设备与技术的服务方案,可省去不必要的沟通时间;在每个阶段我们就为您考虑到下一个阶段快速推进方案,加速您的药品上市进程。